非酒精性脂肪性肝病(NAFLD)及非酒精性脂肪性肝炎(NASH)在全球的患病率以惊人的速度正在增长,患者进一步发展为肝纤维化、肝硬化或肝细胞癌的风险较高。目前,NAFLD患病率占全球人口32.4%,NASH占6.5%,严重威胁着人类健康。NAFLD/NASH发病机制复杂,现在对其认知仍然有限,也没有批准的临床治疗药物。尽管针对NASH的药物研发已经开展了几十年,但由于NASH发病机理不明、缺失适当的动物模型,使得大量的新药研发项目止步于临床开发阶段。因此。构建理想的动物模型是解决NAFLD/NASH威胁的重要挑战与关键环节。

西安交通大学医学部实验动物中心刘恩岐教授联合密西根大学陈育庆教授团队、北京大学郑乐民教授团队,在前期研究的基础上,围绕NAFLD/NASH动物模型开发和新药创制,展开深入研究。项目组首先成功创制了非人灵长类NAFLD/NASH模型,该模型在病理、基因表达、代谢及免疫等方面都与人类NAFLD/NASH非常相似,能够很好的模拟人类疾病病理生理特征,解决了当前NASH新药研发缺失可靠动物模型的这一重要难题和挑战,对NASH新药转化具有重要的意义。
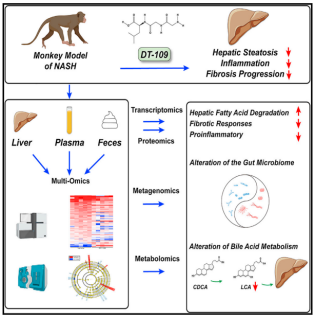
基于动物模型创制的重要突破,尤其是模型动物表现出NASH病人典型的肝脂肪变性、炎症、气球样变、纤维化等病理特征和代谢异常特征。非人灵长类NASH模型促炎和促纤维化通路激活,氨基酸代谢、脂肪酸降解等通路受到抑制,揭示了NAFLD/NASH发生发展过程中的重要基因及关键代谢分子的复杂调控网络。在以上发现基础上,研究人员对潜在的治疗NASH的新药DT109进行了有效性测试,结果显示DT-109能够促进脂肪酸降解和谷胱甘肽形成,通过肠道微生物调控胆汁酸代谢,能够逆转NASH非人类灵长类肝脏脂肪变性、抑制肝纤维化进展。这意味着DT-109作为治疗NASH的潜在候选药物,极有望造福数千万患者。
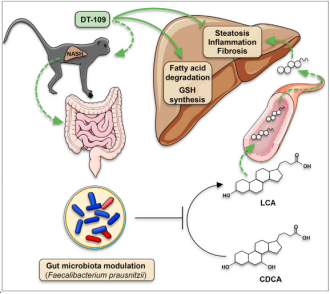
以上研究成果以 “DT-109 ameliorates nonalcoholic steatohepatitis in nonhuman primates”为题近日发表在《Cell Metabolism》杂志。该研究主要工作是在西安交通大学完成的。论文第一作者为西安交通大学医学部实验动物中心屈鹏祥副教授、路易斯安那州立大学Oren Rom助理教授、首都医科大学博士生李科,西安交通大学医学部实验动物中心刘恩岐教授、密西根大学陈育庆教授、密西根大学张继锋副教授、北京大学郑乐民教授为论文的通讯作者;西安交通大学为论文第一作者和通讯作者单位。
该研究工作得到国家重点研发计划、国家自然科学基金、陕西省自然科学基金等支持。
论文链接:https://www.cell.com/cell-metabolism/fulltext/S1550-4131(23)00091-8。